疾患リスト閉じる
- 双胎
- 胸部
- 血液
- 心臓
- 尿路
- 脊椎
胎児疾患HP ・胎児頻脈性不整脈(一般)・胎児頻脈性不整脈(臨床試験)・CDH・TTTS
最終更新日:2020年11月13日
胎児胸水とは胎児の胸腔内(肺の外側)に液体がたまるものです。
原発性胎児胸水とは胸水以外に異常を認めないもので、先天性乳び胸といわれ胎児期に胸腔内にリンパ液が漏れだしてしまう病気です。
頻度は約1万出生に1例といわれています。
胎児胸水は一部に自然に良くなる場合がありますが、良くならずに大量に貯まってしまうと心臓を圧迫して、胎児水腫になります。また肺が長期間圧迫されると肺の発育が阻害され予後は不良です。
胎児の胸腔にカテーテルを留置して胸水を羊水腔内に持続的に排液する胸腔-羊水腔シャント術が、1986年に初めて報告されました。
胸腔-羊水腔シャント術は、心臓と肺への圧迫を除き胎児水腫の改善と肺低形成の予防を目的としています。
最近の報告では、重症の胎児水腫合併の生存率は62%(77/125)で、胎児治療を行わなかった場合の生存率35%(7/20)に比べ有効でした。
日本では1990年頃に、日本独自のダブルバスケットカテーテル(八光商事)が開発されました。
このカテーテルを用いた臨床試験で胸腔-羊水腔シャント術の有用性を示し、2012年7月から胎児胸水に対するシャント術が保険適応となりました。
大量胸水を認めた場合、まず診断と治療を兼ねて胸腔穿刺を行い、1週間以内に再貯留する場合は、重症例と判断され、シャント術を行います。
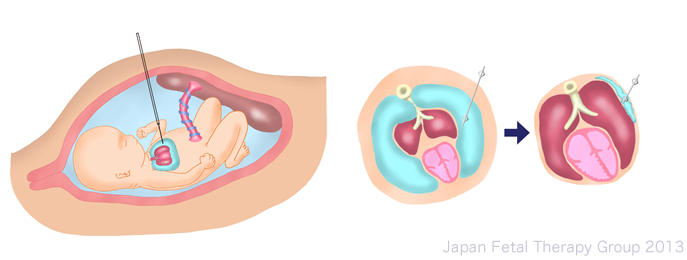
超音波ガイド下で母体腹壁から子宮内の胎児胸腔内と羊水腔を結ぶカテーテルを挿入して、胸水を持続的に羊水腔内へ排液します。
胸水が羊水腔に排液されると、肺がふくらみ、心臓が大きくなります。
やがて徐々に胎児水腫は改善していきます。
しかし、直後には子宮収縮が増強したり、一過性に羊水が増加したりする事もあります。
またチューブが胎動や胎脂などで閉塞したり、抜けてしまったりすることもありますので、術後はしばらく詳細な母児の観察が必要です。
この治療を普及させるために、カテーテルの安全性確認試験の必要性が生じましたので、平成20年4月より22年3月までに「重症胎児胸水に対する胸腔-羊水腔シャント術に関する研究」(厚生労働省科学研究)として臨床試験を実施しました。
全体の生存率は79%(19/24)、胎児水腫例で71%(12/17)、胎児水腫を認めない例では100%(7/7)とこの治療の有効性が示されました。合併症として、シャント術後28日以内の前期破水は4%(1/24)で、またシャントチューブの脱落を10%(4/42)に認めました。日本のダブルバスケットカテーテルを用いたシャント術の有効性と安全性が証明されました。